UP Board Solutions for Class 9 Science Chapter 2 Is Matter Around us Pure
पाठ्य – पुस्तक के प्रश्नोत्तर
पाठगत प्रश्न (पृष्ठ संख्या – 16)
प्रश्न 1.
पदार्थ से आप क्या समझते हैं ?
उत्तर-
पदार्थ वह है जिसमें उपस्थित सभी कण समान रासायनिक प्रकृति के होते हैं।
प्रश्न 2.
समांगी और विषमांगी मिश्रणों में अन्तर बताएँ।
उत्तर-
समांगी मिश्रण – समांगी मिश्रण वह मिश्रण है जिनमें मिश्रित पदार्थों के अवयव समान रूप से मिले होते हैं, समांगी मिश्रण कहलाते हैं।
जैसे-नमक का विलयन, चीनी का विलयन।।
विषमांगी मिश्रण – विषमांगी मिश्रण वह मिश्रण है। जिनमें मिश्रित पदार्थों के अवयव समान रूप से नहीं मिले होते विषमांगी मिश्रण कहलाते हैं।
जैसे- बालू और चीनी का मिश्रण।
पाठगत प्रश्न (पृष्ठ संख्या – 20)
प्रश्न 1.
उदाहरण के साथ समांगी एवं विषमांगी | मिश्रणों में विभेद कीजिए।
उत्तर-
समांगी प्रकृति – द्रव्य की वह स्थिति जिसमें सभी जगह गुण समरूप हों, समांगी प्रकृति कहलाती है। जैसे, चीनी का घोल सर्वत्र समान रूप से मीठा होता है।
अतः चीनी का घोल समांगी है।
विषमांगी प्रकृति – द्रव्य की स्थिति जिसमें एक अंश के गुण दूसरे से भिन्न हों, विषमांगी प्रकृति कहलाती है।
जैसे-मिट्टी युक्त पानी आदि।
प्रश्न 2.
विलयन, निलंबन और कोलॉइड एक-दूसरे से किस प्रकार भिन्न हैं ?
उत्तर-
विलयन, निलंबन और कोलॉइड में निम्न प्रकार से अन्तर स्पष्ट किया जा सकता है
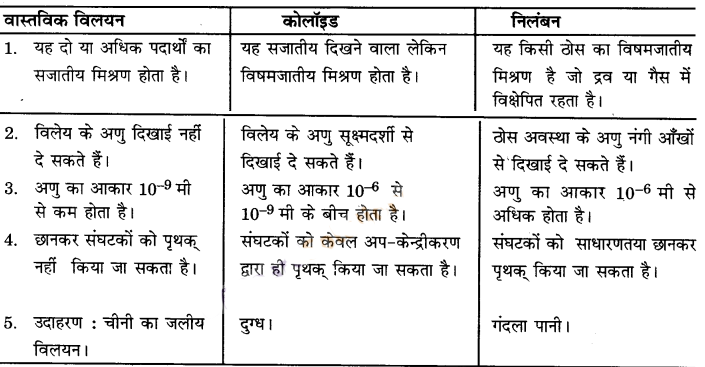
प्रश्न 3.
एक संतृप्त विलयन बनाने के लिए 36 g सोडियम क्लोराइड को 100 g जल में 293 K पर घोला जाता है। इस तापमान पर इसकी सांद्रता प्राप्त करें।
उत्तर-
विलेय (सोडियम क्लोराइड) का द्रव्यमान = 36 g
विलायक (जल) का द्रव्यमान = 100 g
विलयन का द्रव्यमान = विलेय का द्रव्यमान + विलायक का द्रव्यमान = 36 g + 100 g = 136 g

पाठगत प्रश्न (पृष्ठ संख्या – 26)
प्रश्न 1.
पेट्रोल और मिट्टी का तेल (kerosene oil) जो कि आपस में घुलनशील हैं, के मिश्रण को आप कैसे पृथक् करेंगे? पेट्रोल तथा मिट्टी का तेल के क्वथनांकों में 25°C से अधिक का अन्तराल है।
उत्तर-
पेट्रोल और मिट्टी के तेल का पृथक्करण प्रभाजी आसवन विधि द्वारा किया जाता है। दोनों के मिश्रण को प्रभाजी आसवन स्तम्भ में ले जाते हैं फिर ताप को घटाकर उसे ठंडा कर संपीडित किया जाता है जहाँ वाष्प अपने-अपने क्वथनांक के अनुसार पृथक् हो जाती है।
प्रश्न 2.
पृथक् करने की सामान्यविधियों के नाम
(i) दही से मक्खन
(ii) समुद्री जल से नमक
(iii) नमक से कपूर
उत्तर-
(i) दही से मक्खन अपकेन्द्रण द्वारा पृथक् किया जाता है।
(ii) जल से नमक वाष्पीकरण द्वारा पृथक् किया जाता है।
(iii) नमक से कपूर ऊर्ध्वपातन विधि द्वारा पृथक् किया जाता है।
प्रश्न 3.
क्रिस्टलीकरण विधि से किस प्रकार के मिश्रण को पृथक् किया जा सकता है।
उत्तर-
क्रिस्टलीकरण विधि से वे ठोस पदार्थ शुद्ध किये जा सकते हैं, जिनमें अन्य ठोस पदार्थ अशुद्धि के रूप में मौजूद होते हैं।
पाठगत प्रश्न (पृष्ठ संख्या – 27)
प्रश्न 1.
निम्न को रासायनिक और भौतिक परिवर्तनों में वर्गीकृत करें-
पेड़ों को काटना, मक्खन का एक बर्तन में पिघलना, अलमारी में जंग लगना, जल का उबलकर वाष्प बनना, विद्युत तरंग का जल में प्रवाहित होना तथा उसका हाइड्रोजन और ऑक्सीजन गैसों में विघटित होना, जल में साधारण नमक का घुलना, फलों से सलाद बनाना तथा लकड़ी और कागज का जलना।
उत्तर-
भौतिक परिवर्तन – पेड़ों को काटना, मक्खन का एक बर्तन में पिघलना, जल का उबलकर वाष्प बनना, जल में साधारण नमक का घुलना, फलों से सलाद बनाना।
रासायनिक परिवर्तन – अलमारी में जंग लगना, जल में विद्युतधारा का गुजरना तथा उसका हाइड्रोजन और ऑक्सीजन गैसों में विघटित होना, कागज और लकड़ी का जलना।
प्रश्न 2.
अपने आस-पास की चीजों को शुद्ध पदार्थों या मिश्रण से अलग करने का प्रयत्न करें।
उत्तर-
ऑक्सीजन, कॉपर, ऐल्युमिनियम आदि शुद्ध पदार्थ हैं तथा वायु, शर्बत, पीतल आदि मिश्रण हैं।
अभ्यास प्रश्न (पृष्ठ संख्या 30 – 33)
प्रश्न 1.
निम्नलिखित को पृथक् करने के लिए आप किन विधियों को अपनाएँगे ?
(a) सोडियम क्लोराइड को जल के विलयन से पृथक् करने में।
(b) अमोनियम क्लोराइड को सोडियम क्लोराइड तथा अमोनियम क्लोराइड के मिश्रण से पृथक् करने में।
(c) धातु के छोटे टुकड़े को कार के इंजन ऑयल से पृथक् करने में।
(d) दही से मक्खन निकालने के लिए।
(e) जल से तेल निकालने के लिए।
(f) चाय से चाय की पत्तियों को पृथक करने में।
(g) बालू से लोहे की पिनों को पृथक् करने में।
(h) भूसे से गेहूँ के दानों को पृथक् करने में।
(i) पानी में तैरते हुए महीन मिट्टी के कण को पानी से अलग करने के लिए।
(j) पुष्प की पंखुड़ियों के निचोड़ से विभिन्न रंजकों को पृथक् करने में।
उत्तर-
(a) वाष्पीकरण विधि
(b) ऊर्ध्वपातन प्रक्रम
(c) छानने की क्रिया,
(d) अपकेन्द्रीकरण,
(e) कीप-पृथक्करण,
(f) छानने की क्रिया,
(g) चुम्बकीय पृथक्करण,
(h) विनोइंग द्वारा,
(i) निथारने की क्रिया
(j) क्रोमेटोग्राफी प्रक्रम द्वारा।
प्रश्न 2.
चाय तैयार करने के लिए आप किन-किन चरणों का प्रयोग करेंगे?
विलयन, विलायक, विलेय, घुलना, घुलनशील, अघुलनशील, घुलेय, (फिल्ट्रेट) तथा अवशेष शब्दों का प्रयोग करें।
उत्तर-
चाय बनाते समय हम निम्नलिखित चरणों का प्रयोग करेंगे–
चरण-1 : एक पतीली में थोड़ा पानी (विलायक) गर्म करें।
चरण-2 : एक केतली में थोड़ी चाय-पत्तियाँ (विलेय) डालें।
चरण-3 : उबलते पानी को केतली में डाल दें और पत्तियों को कुछ देर फूलने दें। यह एक विलयन में बदल जाएगा।
चरण-4 : एक कप में चीनी (विलेय) डालें । चरण-5 : विलयन को केतली में हिलाएँ।
चरण-6 : छलनी से छानकर विलयन को कप में डालें। दो छोटे चम्मच दूध डालें। चम्मच से मिलाएँ। अब चाय तैयार है। चाय की पत्तियाँ (अवशेष) छलनी में रह जाएँगी जबकि चाय (छना हुआ भाग) विलयन में घुल जाएगी। चीनी और दूध घुलनशील विलेय हैं जबकि चाय की पत्तियाँ अघुलनशील विलेय हैं।
प्रश्न 3.
प्रज्ञा ने तीन अलग-अलग पदार्थों की घुलनशीलताओं को विभिन्न तापमान पर जाँचा तथा नीचे दिए गए आँकड़ों को प्राप्त किया। प्राप्त हुए परिणामों को 100 g जल में विलेय पदार्थ की मात्रा, जो संतृप्त विलयन बनाने हेतु पर्याप्त है, निम्नलिखित तालिका में दर्शाया गया है
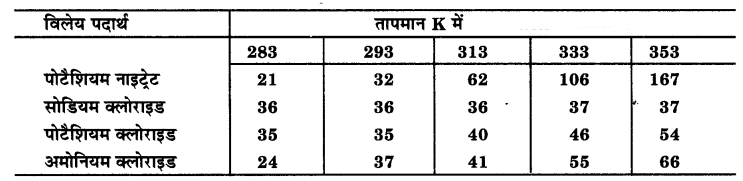
(a) 50 g जल में 313 K पर पोटैशियम नाइट्रेट के संतृप्त विलयन को प्राप्त करने हेतु कितने ग्राम पोटैशियम नाइट्रेट की आवश्यकता होगी ?
(b) प्रज्ञा 358 K पर पोटैशियम क्लोराइड को एक संतृप्त विलयन तैयार करती है और विलयन को कमरे के तापमान पर ठंडा होने के लिए छोड़ देती है। जब विलयन ठंडा होगा तो वह क्या अवलोकित करेगी ? स्पष्ट करें।
(c) 293 K पर प्रत्येक लवण की घुलनशीलता का परिकलन करें। इस तापमान पर कौन-सा लवण सबसे अधिक घुलनशील होगा?
(d) तापमान में परिवर्तन से लवण की घुलनशीलता पर क्या प्रभाव पड़ता है ?
उत्तर-
(a) तालिका के अनुसार, 313 K पर 100 gm जल में 62 gm पोटैशियम नाइट्रेट संतृप्त विलयन बनाने के लिए घोला है।
अतः 50 gm जल में इसका संतृप्त विलयन बनाने के लिए ![]() = 31gm पोटैशियम नाइट्रेट घोलना पड़ेगा।
= 31gm पोटैशियम नाइट्रेट घोलना पड़ेगा।
(b) जब पोटैशियम क्लोराइड के 353 K (80°C) पर संतृप्त घोल को कमरे के तापमान (293 K या 20°C) तक ठंडा किया गया तो उसकी विलेयता घट जाती है और इसके क्रिस्टल पात्र की तली पर इकट्ठा हो जायेंगे।

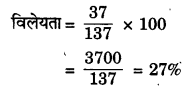
(d) किसी भी पदार्थ की घुलनशीलता तापमान के बढ़ने से बढ़ जाती है।
प्रश्न 4.
निम्नलिखित की उदाहरण सहित व्याख्या कीजिए
(a) संतृप्त विलयन
(b) शुद्ध पदार्थ
(c) कोलाइड
(d) निलम्बने।
उत्तर-
(a) संतृप्त विलयन – किसी दिए हुए तापमान पर जब उस द्रव में और अधिक विलेय पदार्थ न घुल सके उसे संतृप्त घोल कहते हैं।
उदाहरण- कक्ष ताप (20°C) पर 50 mL पानी एक बीकर में लो। अब इसमें सोडियम क्लोराइड (नमक) थोड़ा-थोड़ा करके डालो और घोल लो। ध्यान रहे कि नमक तली में न रहे। इसी प्रकार नमक डालो और हिलाओ। एक स्थिति ऐसी आ जाती है कि और पदार्थ (नमक) घुलना बन्द हो जाता है। यही कक्ष ताप पर संतृप्त विलयन है।
(b) शुद्ध पदार्थ – वे वस्तुएँ जिनका दिए गए तापमान पर रंग-रूप, संरचना, स्वाद व स्वभाव एक समान रहे और उसके हर भाग में संरचना समान हो और उसे सरल
भौतिक विधियों द्वारा और सरल पदार्थों में विभाजित न किया जा सके उसे शुद्ध पदार्थ कहते हैं।
एक शुद्ध पदार्थ या तो तत्त्व होगा या फिर यौगिक।
उदाहरण- सोना, चाँदी, सोडियम, पोटैशियम, कार्बन डाइऑक्साइड आदि शुद्ध पदार्थ हैं।
(c) कोलाइड – यह एक ऐसा विषमांगी मिश्रण है। जिसमें विलेय व विलायक दोनों के कण समान रूप से फैले होते हैं और अधिक देर तक रखने पर भी कण नीचे नहीं बैठते। क्योंकि इनका आकार 1 nm से 100 nm के बीच होता है। ये कोलाइडी कण परिक्षेपण माध्यम में से गुजरने वाले दृश्य प्रकाश का प्रकीर्णन कर देते हैं।
उदाहरण- दूध, स्याही, धुंध, रक्त आदि।
(d) निलम्बन – निलम्बन एक ऐसा विषमांगी मिश्रण है जिसमें विलायक में विलेय पदार्थ घुलता नहीं है और उसके कणों को नंगी आँखों से भी देखा जा सकता है। इसके कणों का आकार 10-5 cm से भी ज्यादा होता है। अधिक देर बिना हिलाए रखने पर कण नीचे बैठ जाते हैं।
उदाहरण- जैसे-चॉक के पाउडर को पानी में विलयन।
प्रश्न 5.
निम्नलिखित में से प्रत्येक को समांगी और विषमांगी मिश्रणों में वर्गीकृत करें-सोडा जल, लकड़ी, बर्फ, वायु, मिट्टी, सिरका, छन्ति चाय।
उत्तर-
समांगी मिश्रण – सोडा जल, सिरका, छनित चाय, बर्फ।
विषमांगी मिश्रण – मिट्टी, लकड़ी।
प्रश्न 6.
आप किस प्रकार पुष्टि करेंगे कि दिया हुआ रंगहीन द्रव शुद्ध जल है?
उत्तर-
रंगहीन तरल पदार्थ किसी भी भौतिक विधि द्वारा और अधिक सरल पदार्थों में विभाजित नहीं किया जा सकता यदि इसे वाष्पित किया जाए तो शेष कुछ नहीं बचता इसलिए दिया गया तरल शुद्ध पदार्थ है।
दिए गए तरल का विद्युत विच्छेदन करने पर हाइड्रोजन तथा ऑक्सीजन आयतन के अनुसार 2 : 1 के अनुपात में प्राप्त होती है अतः दिया गया तरले जल है जो एक यौगिक है। दिया गया तरल वायुमण्डलीय दाब पर 373 K पर उबलने लगता है जो कि शुद्ध जल का क्वथनांक है अतः दिया गया तरल शुद्ध जल है।
प्रश्न 7.
निम्नलिखित में से कौन-सी वस्तुएँ शुद्ध पदार्थ हैं ?
(a) बर्फ
(b) दुध
(c) हाइड्रोक्लोरिक अम्ल
(d) लोहा
(e) कैल्सियम ऑक्साइड
(f) पारा
(g) ईंट
(h) लकड़ी
(i) वायु।
उत्तर-
निम्न शुद्ध पदार्थ’ हैं-
(1) बर्फ
(2) लोहा
(3) हाइड्रोक्लोरिक अम्ल
(4) कैल्सियम ऑक्साइड
(5) पारा
प्रश्न 8.
निम्न मिश्रणों में से विलयन की पहचान करो
(a) मिट्टी
(b) समुद्री जल
(c) वायु
(d) कोयला
(e) सोडा जल।
उत्तर-
विलयन-
(1) समुद्री जल
(2) वायु
(3) सोडा जल
प्रश्न 9.
निम्नलिखित में से कौन टिण्डल प्रभाव को प्रदर्शित करेगा?
(a) नमक का घोल
(b) दूध
(c) कॉपर सल्फेट का विलयन
(d) स्टार्च विलयन
उत्तर-
दूध और स्टार्च विलयन ‘टिंडल प्रभाव दिखाएँगे।
प्रश्न 10.
निम्नलिखित को तत्त्व, यौगिक तथा मिश्रण में वर्गीकृत करें
(a) सोडियम
(b) मिट्टी
(c) चीनी का घोल
(d) चाँदी
(e) कैल्सियम कार्बोनेट
(f) टिन
(g) सिलिकन
(h) कोयला
(i) वायु
(j) साबुन
(k) मीथेन
(l) कार्बन डाइऑक्साइड
(m) रक्त।
उत्तर-
(a) तत्त्व
(b) मिश्रण
(c) यौगिक
(d) तत्त्व
(e) मिश्रण
(f) यौगिक
(g) मिश्रण
(h) मिश्रण
(i) तत्त्व
(j) तत्त्व
(k) तत्त्व
(l) यौगिक
(m) यौगिक।
प्रश्न 11.
निम्नलिखित में से कौन-कौन से परिवर्तन रासायनिक हैं ?
(a) पौधों की वृद्धि
(b) लोहे में जंग लगना
(c) लोहे के चूर्ण तथा बालू को मिलाना
(d) खाना पकाना।
(e) भोजन का पाचन
(f) जल से बर्फ बनना।
(g) मोमबत्ती का जलना।
उत्तर-
लोहे पर जंग लगना, भोजन का पकना, भोजन का पचना और मोमबत्ती का जलना-रासायनिक परिवर्तन हैं।
अन्य महत्वपूर्ण प्रश्नोत्तर
अतिलघु उत्तरीय प्रश्न
प्रश्न 1.
विलयन क्या है ?
उत्तर-
दो या दो से अधिक पदार्थों का समांगी मिश्रण विलयन कहलाता है।
प्रश्न 2.
जलीय विलयन क्या है ?
उत्तर-
विलेय का जल में विलयन, जलीय विलयन कहलाता है।
प्रश्न 3.
संतृप्त विलयन की परिभाषा दीजिए।
उत्तर-
वह विलयन जिसमें किसी ताप पर विलेय की अधिकतम मात्रा घुली हो संतृप्त विलयन कहलाता है।
प्रश्न 4.
विलयन की सान्द्रता से क्या अभिप्राय है?
उत्तर-
विलेय की मात्रा जो विलायक या विलयन की इकाई मात्रा या इकाई आयतन में घुली होती है, विलयन की सान्द्रता कहलाती है।
प्रश्न 5.
कोलाइड काफी स्थायी होते हैं। उस प्रक्रम का नाम बताइये जिससे आप कोलाइड विलयन के अवयवों को पृथक् कर सकते हैं ?
उत्तर-
अपकेन्द्रीकरण द्वारा कोलाइड विलयन के अवयवों को पृथक् कर सकते हैं।
प्रश्न 6.
किस कारक पर आधारित कोई विलयन तनु, सान्द्र अथवा संतृप्त कहलाता है ?
उत्तर-
उसमें उपस्थित विलेय की मात्रा पर आधारित कोई विलयन तनु, सान्द्र अथवा संतृप्त कहलाता है।
प्रश्न 7.
निम्न में से समांगी मिश्रण बताइएलकड़ी, चीनी का जलीय घोल, मिट्टी मिला जल।
उत्तर- चीनी का जलीय घोल।
प्रश्न 8.
केरोसिन तथा जल के मिश्रण को पृथक करने का सिद्धान्त बताइये।
उत्तर-
आपस में नहीं मिलने वाले द्रव अपने घनत्व के अनुसार विभिन्न परतों में पृथक् हो जाते हैं।
प्रश्न 9.
उस प्रक्रम का नाम बताइये जिसे आप जल और ऐल्कोहॉल के मिश्रण को पृथक् करने के लिए प्रयोग करेंगे ?
उत्तर-
ऐल्कोहॉल और जल के मिश्रण को प्रभाजी आसवन द्वारा पृथक् किया जा सकता है।
प्रश्न 10.
30-50 K से अधिक क्वथनांक में अन्तर वाले मिश्रणीय द्रवों को पृथक् करने की विधि का नाम बताइए।
उत्तर-
साधारण आसवन।
प्रश्न 11.
चीनी के संतृप्त विलयन का ताप 5°C `बढ़ाने पर क्या होगा ?
उत्तर-
चीनी के संतृप्त विलयन का ताप 5°C बढ़ाने पर विलयन असंतृप्त हो जायेगा।
प्रश्न 12.
दो अघुलनशील द्रवों को आप किस तकनीक से पृथक् करेंगे ?
उत्तर-
दो अघुलनशील द्रवों को पृथक्करण कीप द्वारा पृथक् करेंगे।
प्रश्न 13.
किसी कोलायडी विलयन में उसके कणों को आकार क्या होगा ?
उत्तर-
कोलाइडी विलयन में कणों का आकार 10-7 cm तथा 10-5 cm के बीच होता है।
प्रश्न 14.
ऊर्ध्वपातन पदार्थ क्या हैं ?
उत्तर-
वह पदार्थ जो गर्म करने से ठोस अवस्था से सीधे गैसीय अवस्था में बदल जाते हैं ऊर्ध्वपातन पदार्थ कहलाते हैं।
प्रश्न 15.
दो ऊर्ध्वपातन पदार्थों के नाम बताइये।
उत्तर-
कपूर और अमोनियम क्लोराइड।
प्रश्न 16.
लोहे की पिन लकड़ी के बुरादे में मिल गयी है, इन्हें कैसे अलग करेंगे? ।
उत्तर-
बुरादे में मिली लोहे की पिनों को चुम्बक द्वारा अलग करेंगे।
प्रश्न 17.
वायु के विभिन्न घटक किस प्रक्रम द्वारा अलग किये जाते हैं ?
उत्तर-
वायु के विभिन्न घटक प्रभाजी आसवन विधि द्वारा अलग किये जाते हैं।
प्रश्न 18.
तन्यता क्या है ?
उत्तर-
धातुएँ खींचने पर तार में बदल जाती हैं, इसे तन्यता कहते हैं।
प्रश्न 19.
टिंडल प्रभाव क्या है ?
उत्तर-
द्रव या गैस में निलम्बित पदार्थ के कणों द्वारा प्रकाश का प्रकीर्णन टिंडल प्रभाव कहलाता है।
प्रश्न 20.
कमरे के ताप पर द्रव अवस्था में पायी जाने वाली धातु का नाम लिखिए।
उत्तर-
कमरे के ताप पर द्रव अवस्था में पायी जाने वाली धातु पारा है।
लघु उत्तरीय प्रश्न
प्रश्न 1.
आसवन को परिभाषित कीजिए। आसवन से किस प्रकार के मिश्रणों को पृथक् किया जा सकता है?
उत्तर-
आसवन, द्रव को गर्म करके वाष्प बनाने और तत्पश्चात् वाष्प को ठंडा करके पुनः द्रव प्राप्त करने का प्रक्रम है। आसवन को विलेय अवाष्पशील ठोसों से द्रव को पृथक् करने के लिए उपयोग किया जा सकता है।
प्रश्न 2.
क्रिस्टलीकरण प्रक्रम क्या है ? यह किस प्रकार उपयोगी है ?
उत्तर-
संतृप्त विलयन में विलेय की अधिकतम मात्रा घुली होती है। अगर विलेय की मात्रा संतृप्त-स्तर से बढ़ जाये तो विलेय की संतृप्त स्तर से अधिक मात्रा अविलेय या क्रिस्टल के रूप में आ जाती है।
अतः संतृप्त विलयन से क्रिस्टल बनने की प्रक्रिया क्रिस्टलीकरण कहलाती है।
उपयोग- यदि कोई पदार्थ ठोस अवस्था में होता है। और उसमें अन्य कोई ठेस अशुद्धि के रूप में पाया जाता है, तब क्रिस्टलीकरण की प्रक्रिया प्रयोग की जाती है।
प्रश्न 3.
5 g विलेय को 40 g जल में घोला गया। है। विलयन की द्रव्यमान प्रतिशतता क्या है?
उत्तर-
विलयन का द्रव्यमान = विलेय का द्रव्यमान + विलायक का द्रव्यमान = 5 g + 40 g = 45 g
विलयन की द्रव्यमान प्रतिशतता

प्रश्न 4.
कोलाइडल विलयन के दो लक्षण लिखिए।
उत्तर-
कोलाइडल विलयन के लक्षण|
(i) कोलाइडी विलयन समांगी दिखाई देता है, परन्तु वास्तव में वह विषमांगी होता है।
(ii) कोलाइडी विलयन में कणों का आकार वास्तविक विलयन से बड़ा परन्तु निलम्बन से छेटा होता है। वह व्यास में 1 nm और 100 nm के बीच होता है।
प्रश्न 5.
मिश्रणीय तथा अमिश्रणीय द्रवों में अन्तर कीजिए।
उत्तर-
मिश्रणीय द्रव-दो या दो से अधिक अमिश्रणीय द्रवों का मिश्रण विभिन्न परतों में पृथक् हो जाता है जिनकी पृथकन सीमाएँ स्पष्ट होती हैं।
अमिश्रणीय द्रव- दो या दो से अधिक मिश्रणीय द्रवों का मिश्रण विभिन्न परतों में पृथक् नहीं होता है और समांगी विलयन बनाते हैं।
प्रश्न 6.
मिश्रणों के प्रकारों को उचित उदाहरण सहित समझाइये।
उत्तर-
अवयवों के मिश्रित होने के आधार पर मिश्रण दो प्रकार के हैं-
(i) समांगी मिश्रण
(ii) विषमांगी मिश्रण।
(i) समांगी मिश्रण : वह मिश्रण जिनमें मिश्रित पदार्थों के अवयव समान रूप से मिले होते हैं समांगी मिश्रण कहलाते हैं, जैसे चीनी को विलयन, नमक का विलयन ।
(ii) विषमांगी मिश्रण : वह मिश्रण जिनमें मिश्रित पदार्थों के अवयव समान रूप से नहीं मिले होते विषमांगी मिश्रण कहलाते हैं, जैसे बालू और चीनी का मिश्रण।
प्रश्न 7.
टिंडल प्रभाव (Tyndall Effect) क्या हैं ?
उत्तर-
टिंडल प्रभाव : जो कोलाइडल कण प्रकाश को एक ओर बिखेरते हैं, उसे टिंडल प्रभाव कहते हैं।
अगर प्रकाश किरण-पुंज को कोलाइड विलयन से गुजारा जाए व प्रकाश किरण के लम्बवत् सूक्ष्मदर्शी रखकर देखा जाए तो प्रकाश किरण का पथ दिखाई देने लगता है।

प्रश्न 8.
आप किसी निलम्बन तथा कोलाइडल में अन्तर किस प्रकार करेंगे ? प्रत्येक का एक-एक उदाहरण दीजिए।
उत्तर-
निलम्बन तथा कोलाइड में अन्तर निम्नलिखित हैं-

प्रश्न 9.
मिश्रण के घटकों को अलग करने की आवश्यकता क्यों पड़ती है ?
उत्तर-
मिश्रण के घटकों को अलग करने की आवश्यकता निम्न कारणों से है :
- अवांछित घटक को दूर करने के लिए।
- किसी हानिकारक घटक को दूर करने के लिए।
- पदार्थ का शुद्ध नमूना प्राप्त करने के लिए।
- किसी लाभप्रद घटक को प्राप्त करने के लिए।
प्रश्न 10.
मिश्रणों के घटकों को पृथक् करने के लिए प्रयोग की जाने वाली सामान्य विधियों के नाम लिखिए।
उत्तर-
मिश्रणों के घटकों को पृथक् करने के लिए। प्रयोग की जाने वाली सामान्य विधियाँ निम्नलिखित हैं :
- छानना
- चुम्बक द्वारा अलग करना
- हाथ से चुनना
- आसवन विधि
- अपकेन्द्रन विधि
- वाष्पीकरण
- ऊर्ध्वपातन की प्रक्रिया द्वारा।
प्रश्न 11.
मिश्रण एवं यौगिक में अन्तर बताइए।
उत्तर-
यौगिक एवं मिश्रण में निम्नलिखित अन्तर है

प्रश्न 12.
क्रोमैटोग्राफी का उपयोग करकेनीली-काली स्याही में उपस्थित राइ को कैसे पृथक् करोगे ?
उत्तर-
- फिल्टर पेपर की एक पतली और लम्बी पट्टी (Strip) लें। इसके निचले किनारे से 3 cm ऊपर पेंसिल से एक रेखा खींचें।
- उस रेखा के बीच में स्याही की एक बूंद रखें। इसे सूखने दें।
- जार में जल लें, उसमें हम फिल्टर पेपर को इस प्रकार रखें कि वह जल की सतह से ठीक ऊपर रहे।
- जैसे ही जल फिल्टर पेपर पर ऊपर की दिशा की ओर अग्रसर होता है यह डाई के कणों को भी अपने साथ ले जाता है। प्रायः डाइ दो या दो से अधिक रंगों का मिश्रण होता है। रंग वाला घटक जो कि जल में अधिक घुलनशील है, तेजी से ऊपर उठता है और इस प्रकार, रंगों का पृथक्करण हो जाता है।
प्रश्न 13.
कैल्सियम कार्बोनेट को गर्म करने पर कैल्सियम ऑक्साइड तथा कार्बन डाइऑक्साइड प्राप्त होते हैं।
(a) क्या यह भौतिक या रासायनिक परिवर्तन है?
(b) उपर्युक्त अभिक्रिया में प्राप्त उत्पादों से क्या तुम एक अम्लीय तथा एक क्षारीय विलयन बना सकते हो? यदि हाँ तो रासायनिक अभिक्रिया का समीकरण लिखिए।
उत्तर-
(a) यह एक रासायनिक परिवर्तन है। (b) हम अम्लीय तथा क्षारीय विलयन बना सकते हैं:
(i) CaO + H2O → Ca(OH)2 (क्षारीय विलयन)
(ii) CO2 + H2O → HaCO3 (अम्लीय विलयन)
प्रश्न 14.
भौतिक एवं रासायनिक परिवर्तन की परिभाषा उदाहरण सहित दीजिए।
उत्तर-
भौतिक परिवर्तन : वह परिवर्तन जिसमें पदार्थ के संघटन में कोई परिवर्तन नहीं होता है भौतिक परिवर्तन कहलाता है। जैसे-जल को बर्फ या भाप में बदलना, विद्युत बल्ब का चमकना।
रासायनिक परिवर्तन : वह परिवर्तन जिसमें पदार्थ के संघटन में परिवर्तन होता है, रासायनिक परिवर्तन कहलाता है। जैसे ईंधन का जलना, लोहे का जंग लगना।
भौतिक परिवर्तन में नया पदार्थ उत्पन्न नहीं होता, केवल पदार्थ के भौतिक गुणों में परिवर्तन होता है, लेकिन रासायनिक परिवर्तन में नया पदार्थ बनता है और पदार्थ के रासायनिक गुणों में परिवर्तन होता है, किसी पदार्थ के रासायनिक गुण उसके रासायनिक संघटन पर निर्भर करते हैं।
प्रश्न 15.
निम्न को भौतिक एवं रासायनिक परिवर्तन में वर्गीकृत करें :
(a) काँच का पिघलना
(b) फूल से फल बनना
(c) अगरबत्ती का जलना
(d) रोटी का पकना
(e) कपड़े का फटना
(f) बादलों का बनना।
उत्तर-
(a) काँच का पिघलना – भौतिक परिवर्तन
(b) फूल से फल बनना – रासायनिक परिवर्तन
(c) अगरबत्ती का जलना – रासायनिक परिवर्तन
(d) रोटी का पकना – रासायनिक परिवर्तन
(e) कपड़े का फटना – भौतिक परिवर्तन
(f) बादलों का बनना – भौतिक परिवर्तन।
दीर्घ उत्तरीय प्रश्न
प्रश्न 1.
विलेय और विलायक की अवस्था के आधार पर विलयनों का वर्णन कीजिए।
उत्तर-
विलेय व विलायक की अवस्था के आधार पर विलयन निम्न प्रकार के हैं :
(i) ठोस का दूर्व में विलयन – जैसे चीनी का जल में विलयन (शर्बत), टिंचर आयोडीन। [आयोडीन (ठोस) का ऐल्कोहॉल (द्रव) में विलयन ।
(ii) गैस का द्रव में विलयन – जैसे ठंडे पेय जिसमें कार्बन डाइऑक्साइड (गैस) जल द्रव में घुली होती है।
(iii) गैस का गैस में विलयन – जैसे वायु जिसमें ऑक्सीजन (21%) व नाइट्रोजन (78%) मिले होते हैं।
(iv) ठोस का ठोस में विलयन – जैसे मिश्र धातुएँ (Alloys)। पीतल में जिंक लगभग 30% व कॉपर लगभग 70% होता है।
प्रश्न 2.
निलम्बन, वास्तविक विलयन व कोलाइडल विलयन को उदाहरण देते हुए परिभाषित कीजिए।
उत्तर-
जब किन्हीं दो पदार्थों का घोल बनता है, तब विलेय के कण परिक्षेपण कण’ (Dispersed particles) व विलायक ‘परिक्षिप्त माध्यम’ (Dispersion medium) कहलाता है।
परिक्षिप्त माध्यम में परिक्षेपण कणों के आकार के आधार पर विलयन तीन प्रकार के हैं-
(i) वास्तविक विलयन : जब परिक्षिप्त माध्यम में परिक्षेपण कणों का व्यास 10-8 सेमी होता है तो परिक्षेपण कण परिक्षिप्त माध्यम में दिखाई नहीं देते। इस प्रकार का विलयन वास्तविक विलयन कहलाता है। उदाहरण- जल में नमक या चीनी का घोल। वास्तविक विलयन में परिक्षेपण कणों को सूक्ष्मदर्शी द्वारा नहीं देखा जा सकता।
(ii) कोलाइडल विलयन : जब परिक्षिप्त माध्यम में परिक्षेपण कणों का व्यास 10-7 से 10-5 सेमी होता है। तो विलयन कोलाइडल विलयन कहलाता है।
उदाहरण- दूध, रक्त, टूथपेस्ट। कोलाइडल विलयन में परिक्षेपण कणों को आँखों द्वारा नहीं देखा जा सकता, लेकिन सूक्ष्मदर्शी द्वारा देखा जा सकता है।
(iii) निलम्बन : जब परिक्षिप्त माध्यम में परिक्षेपण कणों का व्यास 10-5 सेमी या उससे अधिक होता है तो इसे निलम्बन कहते हैं। निलम्बन में परिक्षेपण कणों को परिक्षिप्त माध्यम में तैरते हुए आँख द्वारा देखा जा सकता। है।
उदाहरण- जल में मिट्टी या बालू का घोल, जल में चॉक का घोल।।
प्रश्न 3.
(i) विलयन को परिभाषित कीजिए। जब 15 g NaCl को 200 g जल में घोलकर विलयन तैयार किया जाता है, तो NaCl की द्रव्यमान प्रतिशतता परिकलित कीजिए।
(ii) वास्तविक विलयन से विलेय के कणों को पृथक् करना क्यों असम्भव है ?
(iii) तापमान में परिवर्तन से लवण की घुलनशीलता पर क्या प्रभाव पड़ता है ?
उत्तर-
(i) विलयन : दो या अधिक पदार्थों का समांगी मिश्रण विलयन कहलाता है।
दिया है : NaCl (विलेय) की मात्रा = 15 g
जल (विलायक) की मात्रा = 200 g

(ii) वास्तविक विलयन में विलेय के कणों को पृथक् करना असंभव है, क्योंकि वे विलायक के साथ समांगी मिश्रण बनाते हैं।
(iii) तापमान बढ़ाने पर लवण की घुलनशीलता बढ़ जाती है और घटाने पर कम हो जाती है।
प्रश्न 4.
रासायनिक संघटन के आधार पर शुद्ध पदार्थों के प्रकार का वर्णन कीजिए।
उत्तर-
रासायनिक संघटन के आधार पर शुद्ध पदार्थ दो प्रकार के हैं :
(i) तत्त्व (Element) एवं
(ii) यौगिक (Compound)
(i) तत्त्व : रॉबर्ट बॉयल पहले वैज्ञानिक थे जिन्होंने सन् 1661 में ‘तत्त्व’ शब्द का प्रयोग किया। एंटोनी लॉरेंट लवाइजिए (Antoine Laurent Lavoisier) ने तत्त्व की परिभाषा सर्वप्रथम निम्न प्रकार दी :
“तत्त्व पदार्थ का वह मूल रूप है जिसे रासायनिक क्रिया द्वारा अन्य सरल पदार्थों में विभाजित नहीं किया जा सकता।” जैसे-लोहा, ताँबा, चाँदी ऑक्सीजन, नाइट्रोजन, हाइड्रोजन आदि।
(ii) यौगिक : ‘वह पदार्थ जो दो या अधिक तत्त्वों के किसी निश्चित अनुपात में रासायनिक संयोजन करने से बनता है।”
उदाहरणार्थ
(i) जल एक यौगिक है जो हाइड्रोजन एवं ऑक्सीजन के 1 : 8 के द्रव्यमान-अनुपात में संयोजन करने पर बनता है।
(ii) उसी तरह कार्बन डाइऑक्साइड एक यौगिक है जो कार्बन व ऑक्सीजन के 3 : 8 के द्रव्यमान अनुपात में संयोजन करने से बनती है।
प्रश्न 5.
निम्नलिखित मिश्रण के अवयवों को पृथक् करने की विधि बताइये :
सल्फर + रेत + चीनी + आयरन रेतन।
उत्तर-
इस मिश्रण के चार अवयव हैं-सल्फर, रेत, चीनी तथा आयरन रेतन। मिश्रण के ऊपर से एक चुम्बक को कई बार चलाते हैं। आयरन रेतन, चुम्बक द्वारा आकर्षित हो जाती है। वह चुम्बक पर चिपक जाती है और पृथक् हो जाती है।
चीनी, गंधक तथा रेत के शेष मिश्रण को पानी में डालकर विलोडन करते हैं। इससे जल में चीनी घुल जाती है। छानने पर छनित्र में चीनी का विलयन प्राप्त होता है। छनित्र को वाष्पित करके चीनी प्राप्त की जा सकती है। अवशेष में सल्फर तथा रेत होते हैं।
सल्फर तथा रेत के मिश्रण को कार्बन डाइसल्फाइड के साथ हिलाते हैं जिससे सल्फर, कार्बन डाइसल्फाइड में घुल जाता है और रेत बिना घुले रहता है। छानने पर, सल्फर विलयन के रूप में छनित्र में प्राप्त होती है। कार्बन डाइसल्फाइड के वाष्पन से सल्फर प्राप्त की जा सकती है। रेत, फिल्टर पेपर पर अवशेष के रूप में बच जाता है।
प्रश्न 6.
धातुएँ किसे कहते हैं? इनके गुणधर्मों को समझाइये।
उत्तर-
धातुएँ (Metals) – धातु एक तत्त्व है जो आघातवर्थ्य (malleable) तथा तन्य (ductile) होता है और विद्युत संचालित करता है। धातुओं के कुछ उदाहरण हैं : आइरन, कॉपर, ऐलुमिनियम, जिंक, सिल्वर, गोल्ड, प्लैटिनम, क्रोमियम, सोडियम, पोटैशियम मैग्नीशियम, निकिल, कोबाल्ट, टिन, लेड, कैडमियम, मर्करी, ऐन्टीमनी। एक तत्त्व मर्करी, जो कि एक द्रव है, को छोड़कर सभी धातुएँ ठोस हैं।
धातुओं के गुणधर्म (Properties of Metals)
धातुओं के प्रमुख गुणधर्म नीचे दिये गये हैं :
1. धातुएँ आघातवर्थ्य (malleable) हैं। इसका अर्थ है कि धातुओं को हथौड़े से पतली शीटों में (बिना टूटे) पीटा जा सकता है।
गोल्ड (सोना) तथा सिल्वर (चाँदी) धातुएँ उत्तम आघातवर्थ्य धातुओं में से कुछ हैं। ऐलुमिनियम और कॉपर (ताँबा) धातुएँ भी अत्यधिक आघातवर्थ्य धातुएँ हैं। इन सभी धातुओं को हथौड़े से अत्यंत पतली (महीन) चादरों में कटा जा सकता है जो पन्नी (foils) कहलाती हैं। उदाहरणार्थ, सिल्वर (चाँदी) धातु को, उसकी उच्च आघातवटै र्यता के कारण, हथौड़े से महीन रजत पन्नियों (thin silver foils) में कूटा जा सकता है। चाँदी (रजत) की पन्नियों का उपयोग मिठाइयों को सजाने में किया जाता है। उसी प्रकार, ऐलुमिनियम धातु पर्याप्त आघातवर्थ्य है और महीन शीटों में रूपान्तरित की जा सकती है जो ऐलुमिनियम पन्नियाँ (aluminium foils) कहलाती हैं। ऐलुमिनियम पन्नियों को खाद्य सामग्रियाँ जैसे बिस्कुट, चॉकलेट, दवाइयाँ, सिगरेट इत्यादि पैक करने के लिए उपयोग किया जाता है। दूध की बोतल के ढक्कन भी ऐलुमिनियम पन्नी के बने होते हैं। ऐलुमिनियम चादरों (शीटों) को पाक बर्तनों (cooking utensils) के बनाने में किया जाता है। कॉपर (ताँबा) धातु भी अत्यधिक आघातवर्थ्य है। इसलिए, रसोई या अन्य घरेलू उपयोग के बर्तनों तथा अन्य बर्तनों या पत्रों को बनाने के लिए कॉपर की शीटों (ताँबे की चादरों) का उपयोग किया जाता है। अतः, आघातवर्ध्यता (malleability) धातुओं का एक प्रमुख अभिलाक्षणिक गुणधर्म है।
2. धातुएँ तन्य (ductile) हैं। इसका अर्थ है कि धातुओं को महीन तारों में खींचा जा सकता है। | सभी धातुएँ समान रूप से तन्य नहीं होती हैं। दूसरों की अपेक्षा कुछ अधिक तन्य होती हैं। उत्तम तन्य धातुओं में गोल्ड (सोना) और सिल्वर (चाँदी) हैं। उदाहरणार्थ, सिल्वर जैसी अत्यधिक तन्य धातु के मात्र 100 मिलीग्रामों को लगभग 200 मीटर लम्बे महीन तार में खींचा जा सकता है। कॉपर
और ऐलुमिनियम धातुएँ भी अत्यंत तन्य होती हैं और पतले तारों में खींची जा सकती हैं जिन्हें वैद्युत तार लगाने में उपयोग किया जाता है। अतः, तन्यता (ductility) धातुओं का एक अन्य प्रमुख अभिलाक्षणिक गुणधर्म है।
उपर्युक्त विवेचना से हम निष्कर्ष निकालते हैं कि धातुएँ आघातवर्थ्य और तन्य होती हैं। आघातवर्थ्यता और तन्यता के गुणधर्मों के कारण ही विविध वस्तुएँ बनाने के लिए धातुओं को विभिन्न आकृतियाँ दी जा सकती हैं।
3. धातुएँ ऊष्मा तथा विद्युत की सुचालक हैं। इसका अर्थ है कि धातुएँ ऊष्मा और विद्युत को अपने में से आसानी से प्रवाहित होने देती हैं। धातुएँ सामान्यतः ऊष्मा की सुचालक होती हैं [ऊष्मा का चालन, ऊष्मा चालकता (thermal conductivity) भी कहलाता है। सिल्वर (चाँदी) धातु ऊष्मा का उत्तम चालक है। उसकी सबसे अधिक ऊष्मा चालकता होती है। कॉपर और ऐलुमिनियम धातुएँ भी ऊष्मा की अत्यन्त सुचालक हैं। पाक बर्तनों (cooking utensils) तथा जल क्वथित्रों (water boilers), इत्यादि को प्रायः कॉपर अथवा ऐलुमिनियम धातुओं का बनाया जाता है क्योंकि वे ऊष्मा की अत्यधिक सुचालक होती हैं। धातुओं में ऊष्मा का हीनतम चालक (poorest conductor) लेड (lead) है। मर्करी धातु भी ऊष्मा का हीन चालक है।
4. धातुएँ प्रायः दृढ़ होती हैं। उनमें उच्च तनन सामर्थ्य (high tensile strength) होती है। इसका अर्थ है। कि धातुएँ बिना टूटे भारी (बड़े) भारों को रोक सकती हैं।
उदाहरणार्थ, आइरन धातु (स्टील के रूप में) उच्च | तनन सामर्थ्य वाली अत्यंत दृढ़ होती है। इसके कारण आइरन धातु को सेतुओं या पुलों, भवनों, रेल की पटरियों, गार्डरों, मशीनों, वाहनों और चेनों, इत्यादि के निर्माण में उपयोग किया जाता है। यद्यपि अधिकांश धातुएँ दृढ़ होती हैं। परन्तु कुछ धातुएँ दृढ़ नहीं होती हैं। उदाहरणार्थ, सोडियम और पोटैशियम धातुएँ दृढ़ नहीं हैं। उनमें निम्न तनन सामर्थ्य होती है।
5. धातुएँ कमरे के ताप पर ठोस होती हैं (मर्करी के अतिरिक्त जो कि एक द्रव धातु है।
आइरन, कॉपर, ऐलुमिनियम, सिल्वर तथा गोल्ड, इत्यादि, जैसी सभी धातुएँ कमरे के ताप पर ठोस होती हैं। | कमरे के ताप पर केवल एक धातु, मर्करी, द्रव अवस्था में है।
6. धातुओं का सामान्यतः उच्च गलनांक और क्वथनांक होता है। इसका अर्थ है कि अधिकांश धातुएँ उच्च तापों पर गलती और वाष्पित होती हैं। उदाहरणार्थ, आइरन 1535°C के उच्च गलनांक वाली धातु है। इसका अर्थ है कि 1535°C के उच्च ताप तक गर्म करने पर ठोस आइरन गलता है और द्रव आइरन (अथवा गलित आइरन) में परिवर्तित होता है। कॉपर धातु का भी 1083°C का उच्च गलनांक होता है। यद्यपि, कुछ अपवाद भी हैं। उदाहरणार्थ, सोडियम और पोटैशियम धातुओं के उच्च गलनांक (100°C से कम) होते हैं। अन्य धातु गैलियम का गलनांक इतना कम होता है कि वह हाथ में ही गलने लगता है (हमारे हाथ की ऊष्मा से)।
7. धातुओं के उच्च घनत्व होते हैं। इसका अर्थ है। कि धातुएँ भारी पदार्थ हैं। उदाहरणार्थ, आइरन धातु का घनत्व 7.8 g/cm3 है जो पर्याप्त उच्च है। यद्यपि, कुछ अपवाद हैं। सोडियम और पोटैशियम के निम्न घनत्व होते हैं। वे अत्यंत हल्की धातुएँ हैं।
8. धातुएँ ध्वानिक (sonorous) होती हैं। इसका अर्थ है कि धातुएँ, जब उन्हें मारते हैं, घंटी की ध्वनि उत्पन्न करती हैं। धातुओं के ध्वानिकता के गुण के कारण ही उन्हें घण्टी, प्लेट के प्रकार के बाजा जैसे मंजीरा और तन्तु-वाद्य जैसे वॉयलिन, गिटार, सितार तथा तानपूरा, इत्यादि के लिए तारों (या तंतुओं) को बनाने के लिए उपयोग किया जाता है।
9. धातुएँ प्रायः रजत (silver) अथवा धूसर भूरे (grey) रंग की होती हैं (कॉपर और गोल्ड के अतिरिक्त)। कॉपरे का रक्ताभ भूरा (reddish brown) रंग होता है जबकि गोल्ड (सोने) का रंग पीला होता है।
धातुएँ बहुसंख्यक (अनेक) कार्यों के लिए हमारे दैनिक जीवन में व्यापक रूप से उपयोग की जाती हैं। पाक-उपकरण, बिजली के पंखे, सिलाई मशीनें, कार, बस, ट्रक, रेलगाड़ियाँ, जहाज और वायुयान सभी, धातुओं अथवा मिश्रधातु (alloys) नामक धातुओं के मिश्रण से बनाये जाते हैं। वास्तव में, धातुओं की बनी वस्तुओं की सूची जिन्हें हम अपने दैनिक जीवन में उपयोग करते हैं, अन्तरहित (unending) है।
प्रश्न 7.
अधातुएँ क्या होती हैं? उनके गुणधर्मों को समझाइये।
उत्तर-
अधातुएँ (Non-metals) : अधातु एक तत्त्व है जो न तो आघातवर्थ्य न तनय होता है, और विद्युत चालित (प्रवाहित) नहीं करता है। अधातुओं के कुछ उदाहरण हैं : कार्बन, सल्फर, फॉस्फोरस, हाइड्रोजन, ऑक्सीजन, नाइट्रोजन, फ्लुओरीन, क्लोरीन, ब्रोमीन, आयोडीन, हीलियम, निऑन, ऑर्गन, क्रिप्टान, और जीनाने । हीरा (diamond) तथा ग्रेफाइट (graphite) भी अधातुएँ हैं। वे कार्बन के अपररूप (allotropic forms) हैं। कमरे के ताप पर सभी अधातुएँ, ब्रोमीन के अतिरिक्त जो एक द्रव अधातु है, ठोस (solids) अथवा गैस (gases) होती हैं।
अधातुओं के गुणधर्म (Properties of Nonmetals) :
अधातुओं के भौतिक गुणधर्म, धातुओं के भौतिक गुणधर्मों के बिल्कुल विपरीत हैं। अधातुओं के प्रमुख भौतिक गुणधर्म नीचे दिये गये हैं :
1. अधातुएँ आघातवर्थ्य नहीं हैं। अधातुएँ भंगुर (brittle) होती हैं। इसका अर्थ है कि अधातुओं को हथौड़े से पतली चादरों (thin sheets) में नहीं पीटा जा सकता है। जब हथौड़ा मारा जाता है, अधातुएँ छोटे-छोटे टुकड़ों में टूट जाती हैं।
उदाहरणार्थ, सल्फर (गंधक) और फॉस्फोरस ठोस अधातुएँ हैं जो आवातवर्थ्य नहीं हैं, उन्हें हथौड़े से पतली चादरों में पीटा नहीं जा सकता है। अतः अधातुओं की हम पतली चादरें नहीं प्राप्त कर सकते हैं। सल्फर और फॉस्फोरस अधातुएँ भंगुर हैं। हथौड़े से जब पीटी जाती हैं, वे छोटे-छोटे टुकड़ों में टूट जाती हैं। भंगुरता (brittleness) ठोस अधातुओं का अभिल्लाक्षणिक गुणधर्म है।
2. अधातुएँ तन्य नहीं होती हैं। इसका अर्थ है कि अधातुओं को तारों में र्वीचा नहीं जा सकता है। खींचने पर वे आसानी से पड़-पड़ करके टूट जाती हैं।
उदाहरणार्थ, सल्फर और फॉस्फोरस अधातुएँ हैं और वे तन्य नहीं हैं। जब खींचा जाता है, सल्फर और फॉस्फोरस
टुकड़ों में टूट जाते हैं और तार नहीं बनाते हैं। अतः अधातुओं से हम तार नहीं प्राप्त कर सकते हैं। उपर्युक्त विवेचना से हम निष्कर्ष निकालते हैं कि : अधातुएँ न तो आघातवष्ट ये हैं न तन्य। अधातुएँ भंगुर हैं।
3. अधातुएँ ऊष्मा और विद्युत की कुचालक होती हैं। इसका अर्थ है कि अधातुएँ अपने में से ऊष्मा और विद्युत को प्रवाहित नहीं होने देती हैं। अधातुओं में से अनेक, वास्तव में, विद्युतरोधी (insulators) हैं। यद्यपि, कुछ अपवाद हैं। कार्बन तत्त्व का एक रूप, हीरा (diamond) अधातु है जो ऊष्मा का सुचालक है और कार्बन तत्त्व का एक अन्य रूप, ग्रेफाइट अधातु है जो विद्युत का सुचालक है। विद्युत का सुचालक होने से, ग्रेफाइट इलेक्ट्रोड (eletrodes) बनाने के लिए उपयोग किया जाता है (जैसे कि शुष्क सेलों में)।
4. अधातुएँ दीप्त (या चमकीली) नहीं होती हैं। वे देखने में धुंधली होती हैं। अधातुओं में चमक नहीं होती। है जिसका मतलब है कि अधातुओं में चमकीली सतह नहीं होती है। ठोस अधातुएँ देखने में धुंधली होती हैं। उदाहरणार्थ, सल्फर और फॉस्फोरस अधातुएँ हैं जिनमें दीप्ति । (चमक) नहीं है, अर्थात्, उनमें चमकीली सतह नहीं होती है। वे धुंधली (भद्दी) प्रतीत होती हैं। यद्यपि, एक अपवाद है। आयोडीन दीप्त (चमकीली) आकृति वाली अधातु होती है। उसमें चमकीली ऊपरी सतह होती है (धातुओं की भाँति)।
5. अधातुएँ आमतौर पर मृदु होती हैं (हीरे के अतिरिक्त क्योंकि यह अत्यंत कठोर अधातु है)। अधिकांश ठोस अधातुएँ काफी मृदु होती हैं। वे चाकू से आसानी से कट सकती हैं। उदाहरणार्थ, सल्फर और फॉस्फोरस ठोस अधातुएँ हैं जो काफी मृदु हैं और चाकू से आसानी से काटी जा सकती हैं। केवल एक अधातु कार्बन (हीरे के रूप में) अत्यंत कठोर है। वास्तव में, हीरा (जो कार्बन का एक अपररूप है। ज्ञात कठोरतम प्राकृतिक पदार्थ है।
6. अधातुएँ दृढ़ नहीं होती हैं। उनमें निम्न तनन सामर्थ्य होती है। इसका अर्थ है कि अधातुएँ बड़े (भारी) भारों को (बिना टूटे) रोक नहीं सकती हैं। उदाहरणार्थ, ग्रेफाइट एक अधातु है जो दृढ़ नहीं है। उसमें निम्न तनन सामर्थ्य होती है। जब ग्रेफाइट चादर पर भारी भार रखा जाता है, वह टूट जाता है।
7. अधातुएँ, कमरे के ताप पर, ठोस, द्रव अथवा गैसें हो सकती हैं। अधातुएँ सभी तीन अवस्थाओं : ठोस, द्रव और गैस में हो सकती हैं। उदाहरणार्थ, कार्बन, सल्फर और फॉस्फोरस ठोस अधातुएँ हैं; ब्रोमीन द्रव अधातु है; जबकि हाइड्रोजन, ऑक्सीजन, नाइट्रोजन और क्लोरीन गैसीय अधातुएँ हैं।
8. अधातुओं के, तुलनात्मक रूप से, निम्न गलनांक और क्वथनांक होते हैं (ग्रेफाइट के अतिरिक्त जो अत्यंत उच्च गलनांक वाली अधातु है)। इसका मतलब है यह कि अधातुएँ, तुलनात्मक रूप से निम्न तापों पर गलती और वाष्पित होती हैं।
उदाहरणार्थ, सल्फर 119°C के निम्न गलनांक वाली अधातु है। आयोडीन भी 113°C के निम्न गलनांक वाली अधातु है। केवल एक अधातु ग्रेफाइट का अत्यंत उच्च गलनांक (3700°C) होता है। अधिकतर अधातुओं के अत्यंत निम्न गलनांक होते हैं जिसके कारण वे कमरे के ताप पर गैसों के रूप में उपस्थित होते हैं।
9. अधातुओं के निम्न घनत्व होते हैं। इसका अर्थ है। कि अधातुएँ हल्के पदार्थ हैं। उदाहरणार्थ सल्फर 2 g/cm3 के निम्न घनत्व वाला ठोस अधातु है, जो काफी निम्न है। गैसीय अधातुओं का घनत्व अत्यंत निम्न होता है। एक अधातु आयोडीन का यद्यपि, उच्च घनत्व होता है।
10. अधातुएँ वानिक sonorous) नहीं होती हैं। इसका अर्थ है कि ठोस अधातुएँ, जब उन्हें मारा जाता है, घण्टी की ध्वनि उत्पन्न नहीं करती हैं।
प्रश्न 8.
कोलाइडों का संक्षिप्त वर्णन कीजिए।
उत्तर-
कोलाइडों को निम्नलिखित सात वर्गों में वर्गीकृत किया जा सकता है
(i) सॉल (Sol)
(ii) ठोस सॉल (Solid sol)
(iii) ऐरोसॉल (Aerosol)
(iv) इमल्शन (Emulsion)
(v) फोम (Foam)
(vi) ठोस फोम (Solid Foam)
(vii) जेल (Gel)
(i) सॉल (Sol) – सॉल एक कोलाइड है जिसमें नन्हें ठोस कण, द्रव माध्यम में परिक्षिप्त होते हैं। सॉलों के उदाहरण हैं : स्याही, साबुन विलयन, स्टार्च विलयन और अधिकांश पेण्ट (प्रलेप)
(ii) ठोस सॉल (Solid Sol) – ठोस सॉल एक कोलाइड है जिसमें ठोस कण, ठोस माध्यम में परिक्षिप्त होते हैं। ठोस सॉल का उदाहरण है : रंगीन रत्नपत्थर (माणिक्य काँच के समान) ।।
(iii) ऐरोसॉल (Aerosol) – ऐरोसॉल एक कोलाइड है जिसमें ठोस अथवा द्रव, गैस (वायु सहित) में परिक्षिप्त होता है। कोलाइडों जिनमें गैस में ठोस परिक्षिप्त होता है, के उदाहरण हैं : धुआँ या धूम (जो वायु में कालिख है) और स्वचालित वाहन निष्कास (Automobile Exhausts)। ऐरोसॉलों जिनमें गैस में द्रव परिक्षिप्त होता है, के उदाहरण हैं : केश स्प्रे, कोहरा, कुहासा और मेघ या बादल।
(iv) इमल्शन (Emulsion) – इमल्शन (पायस) एक कोलाइड है जिसमें एक दूव की अत्यंत छोटी सूक्ष्म बूंदें, दूसरे द्रव जो उसके साथ मिश्रणीय नहीं हैं, में परिक्षिप्त होती हैं। इमल्शन के उदाहरण हैं दूध, मक्खन और फेस क्रीम।
(v) फोम (Foam) – फोम (फेन या झाग) एक कोलाइड है जिसमें ठोस माध्यम में गैस परिक्षिप्त होती है। फोम के उदाहरण हैं : अग्निशामक आग (Fire-extinguisher Foam); साबुन के बुलबुले (Soap Bubbles), शेविंग क्रीम (Shaving Cream) और बीअर झाग (Beer Foam)।
(vi) ठोस फोम (Solid Foam) – ठोस फोम एक कोलाइड है जिसमें ठोस माध्यम में गैस परिक्षिप्त होती है। ठोस फोम के उदाहरण हैं : रोधी फोम, फोम रबड़ और स्पंज।
(vii) जेल (Gel) – जेल एक अर्द्ध-ठोस कोलाइड है जिसमें द्रव में परिक्षिप्त ठोस कणों को लगातार जलक होता है। जेल के उदाहरण हैं : जेलियाँ (Jellies) और जिलैटिन (Gelatine)
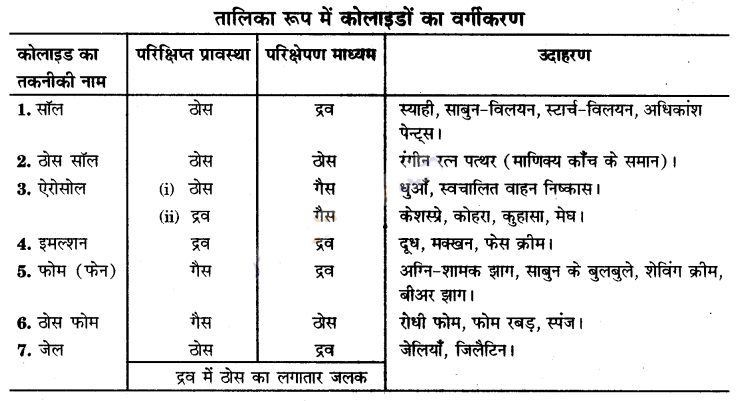
प्रश्न 9.
एक विलयन में, जल के 370 g में शक्कर के 30 ग्राम घुले हुए हैं। इस विलयन के सान्द्रण (सान्द्रता) की गणना कीजिए।


अभ्यास प्रश्न
बहुविकल्पीय प्रश्न
1. लोहे से बने किसी बर्तन पर जंग का लगना कहलाता है
(a) घुलना और यह एक भौतिक परिवर्तन
(b) संक्षारण और यह एक रासायनिक परिवर्तन
(c) घुलना और यह एक रासायनिक परिवर्तन
(d) उपर्युक्त में से कोई नहीं।
2. सल्फर तथा कार्बन डाइसल्फाइडे का मिश्रण है
(a) समांगी तथा टिण्डल प्रभाव नहीं दर्शाता है।
(b) विषमांगी तथा टिण्डल प्रभाव नहीं दर्शाता है।
(c) समांगी तथा टिण्डल प्रभाव देर्शाता है।
(d) उपर्युक्त में से कोई नहीं।
3. समुद्री जल से नमक प्राप्त किया जाता है|
(a) वाष्पीकरण द्वारा
(b) प्रभाजी आसवन द्वारा
(c) क्रोमैटोग्राफी द्वारा
(d) अपकेन्द्रन विधि द्वारा।
4. ऊर्ध्वपातन पदार्थ नहीं है
(a) आयोडीन
(b) बेंजीन
(c) कपूर
(d) अमोनियम क्लोराइड।
5. पृथक्करण फनल का उपयोग करते हैं अलग करने के लिए
(a) दो घुलनशील द्रवों को
(b) द्रव में अघुलनशील कणों को
(c) दो अघुलनशील द्रवों को।
(d) द्रव में विलेय ठोस पदार्थ को।
6. लोहे की पिने, बालू व अमोनियम क्लोराइड के मिश्रण घटकों को अलग करने के लिए प्रयोग किये गये प्रक्रमों का सही क्रम है
(a) विलयन बनाना, छानना व चुम्बकीय पृथक्करण
(b) चुम्बकीय पृथक्करण, विलयन बनाना व छानना
(c) चुम्बकीय पृथक्करण, ऊर्ध्वपातन
(d) विलयन बनाना, आसवन व चुम्बकीय पृथक्करण
7. गर्म करने पर सन्तृप्त विलयन हो जायेगा|
(a) अति सन्तृप्त
(b) असन्तृप्त
(c) अपघटित
(d) तनु विलयन।
8. टिंडल प्रभाव प्रदर्शित नहीं करते हैं
(a) वास्तविक विलयन
(b) निलम्बन
(c) कोलाइडल
(d) ये सभी।
9. क्रोमैटोग्राफी का प्रयोग करते हैं
(a) डाई में रंगों को अलग करने में
(b) प्राकृतिक रंगों से लवकों को अलग करने में
(c) रक्त से नशीले पदार्थों को दूर करने में।
(d) उपर्युक्त सभी में।
10. धातुएँ
(a) चमकीली व गहरे रंग की होती हैं।
(b) विद्युत व ताप की सुचालक होती हैं।
(c) आघातवर्थ्य एवं तन्य होती हैं।
(d) उपर्युक्त सभी।
11. कमरे के ताप पर द्रव धातु है
(a) टिन
(b) ब्रोमीन
(c) पारा
(d) बोरॉन
12. कमरे के ताप पर द्रव अधातु है
(a) टिन
(b) ब्रोमीन
(c) पारा
(d) बोरॉन
13. उपधातु का उदाहरण है
(a) टिन
(b) ब्रोमीन
(c) पारा
(d) बोरॉन।
14. दो घुलनशील द्रव अलग किये जाते हैं
(a) आसवन प्रक्रम द्वारा
(b) पृथक्करण फनल द्वारा
(c) भारण विधि द्वारा
(d) ऊर्ध्वपातन द्वारा।
15. निलम्बन के कण दूर किये जाते हैं
(a) आसवन द्वारा
(b) पृथक्करण फनल द्वारा
(c) भारण विधि द्वारा
(d) ऊर्ध्वपातन द्वारा।
16. दो अघुलनशील द्रव अलग किये जाते हैं
(a) आसवन द्वारा
(b) पृथक्करण फनले द्वारी
(c) भारण विधि द्वारा
(d) ऊर्ध्वपातन द्वारा।
17. दूध से क्रीम निकाली जाती है|
(a) आसवन द्वारा
(b) प्रभाजी आसवन द्वारा
(c) क्रोमैटोग्राफी द्वारा
(d) अपकेन्द्रन विधि द्वारा।
18. पेट्रोलियम व वायु के घटक प्राप्त किये जाते हैं
(a) आसवन द्वारा
(b) प्रभाजी आसवन द्वारा ।
(c) क्रोमैटोग्राफी द्वारा
(d) अपकेन्द्रन विधि द्वारा।
19. रक्त से नशीले पदार्थ अलग किये जाते हैं
(a) वाष्पीकरण द्वारा
(b) प्रभाजी आसवन द्वारा
(c) क्रोमैटोग्राफी द्वारा
(d) अपकेन्द्रन विधि द्वारा।
20. घटकों का पृथक्करण चाहिए|
(a) अवांछित या हानिकारक घटक को दूर करने के लिए
(b) शुद्ध पदार्थ प्राप्त करने के लिए
(c) लाभदायक घटक को प्राप्त करने के लिए
(d) उपर्युक्त सभी
21. समांगी मिश्रण का उदाहरण है
(a) कॉपर सल्फेट का विलयन
(b) नमक व सल्फर का मिश्रण
(c) सल्फर व लोहे के चूर्ण का मिश्रण
(d) उपर्युक्त सभी।
22. दो या अधिक पदार्थों को समांगी मिश्रण कहलाता
(a) विलयन
(b) निलम्बन
(c) कोलाइडल
(d) इनमें से कोई भी नहीं।
23. निलम्बन है एक
(a) समांगी मिश्रण
(b) विषमांगी मिश्रण जिसमें घुलित कण आँखों से देखे जा सकें
(c) विषमांगी मिश्रण जिसमें घुलित कण आँखों से न देखे जा सकें
(d) उपर्युक्त सभी।
24. विलयन है एक
(a) समांगी मिश्रण
(b) विषमांगी मिश्रण जिसमें घुलित कण आँखों से देखे जा सकें
(c) विषमांगी मिश्रण जिसमें घुलित कण आँखों से न देखे जा सकें
(d) उपर्युक्त सभी।
25. कोलाइडल है एक
(a) समांगी मिश्रण
(b) विषमांगी मिश्रण जिसमें घुलित कण आँखों से देखे जा सकें
(c) विषमांगी मिश्रण जिसमे घुलित कण आँखों से न ‘ देखे जा सकें।
(d) उपरोक्त सभी।
26. मिश्रण के विषय में सही कथन नहीं है।
(a) घटक अपने गुण प्रदर्शित करते हैं।
(b) मिश्रण के गुण घटकों के गुण से भिन्न होते हैं।
(c) घटक किसी भी अनुपात में मिले होते हैं।
(d) घटक सरल विधियों द्वारा अलग किये जा सकते हैं।
27. विषमांगी मिश्रण का उदाहरण है
(a) लकड़ी
(b) पीतल
(c) नमक का जलीय विलयन
(d) स्टील।
28. ठोस-ठोस विलयन का उदाहरण है–
(a) लकड़ी
(b) पीतल
(c) नमक का जलीय विलयन
(d) इमल्शन।
29. गंदला पानी उदाहरण है
(a) विलयन का
(b) निलम्बन का
(c) कोलाइडल का
(d) ये सभी
30. साबुन का जलीय विलयन है एक
(a) विलयन का
(b) निलम्बन का
(c) कोलाइडल का
(d) ये सभी ।
उत्तरमाला
- (b)
- (a)
- (a)
- (b)
- (c)
- (c)
- (b)
- (a)
- (d)
- (d)
- (c)
- (b)
- (d)
- (a)
- (c)
- (b)
- (d)
- (b)
- (c)
- (d)
- (a)
- (a)
- (b)
- (a)
- (c)
- (b)
- (a)
- (b)
- (b)
- (c)
We hope the UP Board Solutions for Class 9 Science Chapter 2 Is Matter Around us Pure (क्या हमारे आस-पास के पदार्थ शुद्ध हैं) help you.